De zuurtegraad aanpakken: een nieuwe manier om alvleesklierkanker te bestrijden
Het remmen van de bicarbonaattransporter SLC4A4 in alvleesklierkankercellen bevordert een immuunreactie en ondersteunt de effectiviteit van immunotherapie.
Een type pancreaskanker dat bekend staat als pancreasadenocarcinoom (PDAC) is een van de meest agressieve en dodelijke vormen van kanker. Huidige vormen van immunotherapie werken niet. Onderzoek door het team van prof. Massimiliano Mazzone (VIB-KU Leuven Centrum voor Kankerbiologie), KU Leuven, UZ Leuven en internationale collega's identificeerde een nieuw therapeutisch doelwit. Door de zuurgraad van de micro-omgeving van de tumor te veranderen verhinderen de onderzoekers de onderdrukking van het immuunsysteem en immunotherapieresistentie. Hun werk verschijnt in Nature Cancer.
In het kort:
- Alvleesklierkanker heeft het hoogste sterftecijfer van alle vormen van kanker. Voor alle stadia samen is het relatieve overlevingspercentage na 5 jaar 11%.
- Pancreasadenocarcinoom (PDAC) is verantwoordelijk voor meer dan 90% van de alvleesklierkankers.
- PDAC-tumoren vertonen een sterke daling van de pH van de vloeistof tussen cellen – ze bevinden zich in een meer zure omgeving in vergelijking met normale weefsels.
- Het onderdrukken van de bicarbonaattransporter SLC4A4 verhoogt de pH (= minder zuur) van de tumoromgeving, wat de antitumorimmuniteit ondersteunt en doeltreffendheid verleent aan immunotherapie.
Zure omgevingen helpen tumoren te ontsnappen aan het immuunsysteem
Tumoren verlagen meestal de pH in hun omgeving vanwege hun snelle metabolisme. Het resultaat is een zure micro-omgeving van de tumor. Dit is met name het geval bij pancreasadenocarcinoom (PDAC), een van de meest agressieve en dodelijke vormen van kanker. Tot nu toe hebben conventionele therapieën en immunotherapie weinig verlichting gebracht voor PDAC-patiënten. De zure micro-omgeving van de tumor kan hier de oorzaak van zijn. Het onderdrukt de lichaamseigen afweerreactie en vermindert de effectiviteit van immunotherapie.
Prof. Mazzone (VIB-KU Leuven Centrum voor Kankerbiologie): "Vanwege de rol die pH speelt in de immuunrespons, hebben we besloten om bicarbonaattransporters - die helpen bij het reguleren van de pH in het lichaam - nader te onderzoeken bij de progressie en controle van de immuunrespons in PDAC. Door datasets van PDAC-patiënten te analyseren, hebben we ons met name gericht op de meest tot expressie gebrachte transporter in pancreascellen, genaamd SLC4A4."
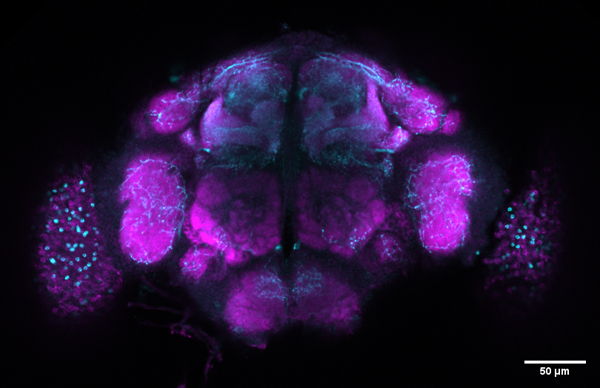
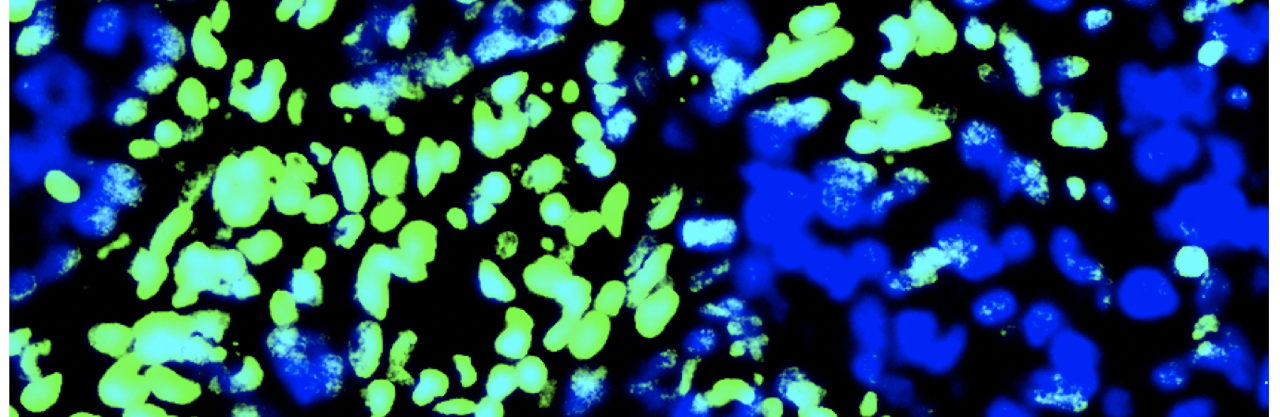
Links: identificatie van slc4a4 in ductale cellen van alvleesklierkankerpatiënten; rechts: transcriptomische analyse maakt doeldetectie mogelijk bij PDAC-patiënten.
Zuurgraad verlagen
In zowel celculturen als muismodellen toont het team van prof. Massimiliano Mazzone (VIB-KU Leuven Centrum voor Kankerbiologie), KU Leuven, UCL Leuven, Universitair Ziekenhuis Leuven en internationale collega's aan dat het blokkeren van SLC4A4 op kankercellen de immuunrespons verbetert en immunotherapie stimuleert. Normaal gesproken zorgt deze transporter ervoor dat de tumorcellen bicarbonaat uit de omgeving kunnen opnemen. Dit verlaagt de pH van de omgeving en maakt het zuurder. Door de transporter te blokkeren blijft het bicarbonaat in de omgeving van de tumor, die daardoor minder zuur wordt. Een minder zure micro-omgeving van de tumor is gastvrijer voor immuuncellen die zich op de tumor kunnen richten.
Federica Cappellesso, eerste auteur van de studie: "Toen we SLC4A4 blokkeerden in muizen met PDAC-tumoren, zagen we verbeteringen in de immuunreactie die tumorgroei en metastase voorkomen. We vonden ook een betere respons op immunotherapie. SLC4A4 lijkt een geweldig therapeutisch middel te zijn om een anti-tumor immuunrespons te bekomen bij pancreaskanker."

Van wetenschappelijke ontdekking tot therapieontwikkeling
Geïnspireerd door de preklinische bevindingen over de rol van SCL4A4 in PDAC, bundelde VIB Discovery Sciences (VDS) hun krachten met het team van prof. Mazzone om biologische kandidaat-geneesmiddelen te ontdekken en te karakteriseren die SLC4A4 selectief kunnen remmen. Veelbelovende resultaten in celculturen en muismodellen moedigden het team aan om dit project voort te zetten naar de vroege ontwikkeling van geneesmiddelen. Er zijn nog verschillende stappen te nemen voordat we tot een medicijn voor menselijke patiënten komen, maar het team is hoopvol en gemotiveerd.
De VDS-eenheid is een translationeel onderzoeksteam van wetenschappers en technici met een sterke achtergrond in de biotechnologie-industrie. Ze helpen de wetenschappelijke doorbraken van VIB-wetenschappers te valideren en richten zich op de vertaling van vroeg onderzoek naar therapeutische en diagnostische producten voor toepassing in de medische en landbouwsector.
Publicatie
Targeting the bicarbonate transporter SLC4A4 overcomes immunosuppression and immunotherapy resistance in pancreatic cancer. Cappellesso et al. Nature Cancer, 2022.
Vragen van patiënten
Een doorbraak in onderzoek is niet hetzelfde als een doorbraak in de geneeskunde. De realisaties van VIB-onderzoekers kunnen de basis vormen van nieuwe therapieën, maar het ontwikkelingstraject duurt nog jaren. Dit kan veel vragen oproepen. Daarom vragen we je vragen in je verslag of artikel te verwijzen naar het e-mailadres dat VIB hiervoor ter beschikking stelt: patienteninfo@vib.be. Via dit adres kan iedereen rechtstreeks met VIB terecht met vragen over dit en ander medisch gericht onderzoek.
Over het VIB-KU Leuven Centrum voor Kankerbiologie
Kanker heeft vele oorzaken. Vaak is het een combinatie van levensstijl, omgevingsfactoren en genetische variatie. We moeten kanker op veel fronten bestrijden en dat kan alleen met behulp van kennis. De onderzoekers van het VIB-KU Leuven Centrum voor Kankerbiologie ontrafelen nieuwe mechanismen om zowel specifieke diagnostische methodes als behandelingen te ontwikkelen.
Gunnar De Winter
.png)