Hoe afvalophoping in hersencellen kan leiden tot Alzheimer
Leuven, 25 mei 2023 - Hoewel miljoenen mensen getroffen worden door de ziekte van Alzheimer, zijn er nog veel vragen over de onderliggende oorzaken van deze aandoening. In hun meest recente onderzoek hebben wetenschappers van het laboratorium van Wim Annaert (VIB-KU Leuven) een stukje van de puzzel ontrafeld door uit te leggen hoe een genetische variatie in het 'afvalophaal- en verwerkingssysteem' van hersencellen kan leiden tot Alzheimer.
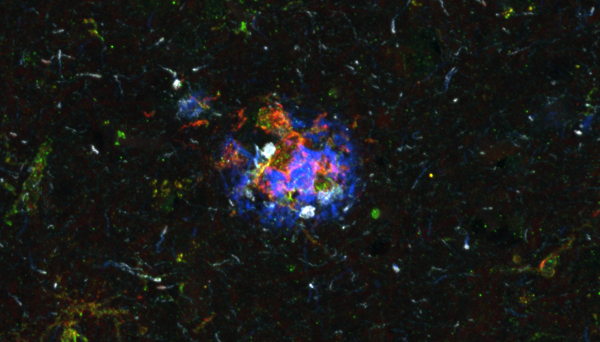
Bij de ziekte van Alzheimer wordt het amyloïde voorlopereiwit in de hersenen verkeerd verwerkt, waardoor schadelijke eiwitfragmenten ontstaan. Deze kunnen zich ophopen in de hersenen en plaques vormen. De ophoping van deze fragmenten begint al vroeg in de ziekte, zelfs vele jaren voordat de eerste klinische symptomen bij patiënten ontstaan. Dit is grotendeels te wijten aan het feit dat breincellen geleidelijk het vermogen verliezen om dit celafval te vernietigen.
Het afbraaksysteem van hersencellen, ook wel het lysosomale systeem genoemd, speelt een belangrijke rol bij het opruimen en recycleren van oude of beschadigde componenten. Het helpt de hersencellen gezond te houden door de opstapeling van schadelijk afval te vermijden. Een gezond lysosomaal systeem is dan ook essentieel voor het levenslang goed functioneren van onze hersenen.
Naarmate we ouder worden, wordt dit lysosomale systeem kwetsbaarder. In de vroege stadia van neurodegeneratieve ziekten zoals de ziekte van Alzheimer wordt dit proces ook nog eens versneld. Het is dan ook niet verwonderlijk dat dat verschillende risicogenen voor de ziekte van Alzheimer in verband zijn gebracht met het functioneren van het lysosomale systeem. Maar we begrijpen nog niet volledig hoe deze genen ervoor zorgen dat het lysosomale systeem faalt.
Eén van deze genen, genaamd PLD3, is onderzocht door Wim Annaert en zijn team. Mensen met Alzheimer hebben minder van dit eiwit, en sommigen hebben zelfs bepaalde varianten van het PLD3-gen die het risico op de ziekte vergroten.
“We weten nog heel weinig over hoe exact bepaalde genen het risico op Alzheimer verhogen. Om de ziekte te begrijpen, is het echter essentieel om te weten hoe de betrokken eiwitten werken in de hersencellen. Voor één van deze genen, PLD3, hebben we nu ontdekt hoe het falen ervan in lysosomen verband houdt met de ziekteverschijnselen van Alzheimer.” - Wim Annaert (VIB-KU Leuven)

Een lek dat tot verstopping leidt
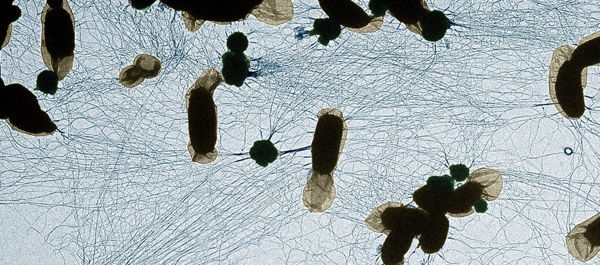
Eerder onderzoek toonde al aan dat PLD3 sterk aanwezig was in de lysosomen van het brein, waar het helpt DNA-fragmenten af te breken in breincellen. Waarom deze DNA-fragmenten daar aanwezig waren en wat het verband was met Alzheimer, was echter nog een vraagteken.
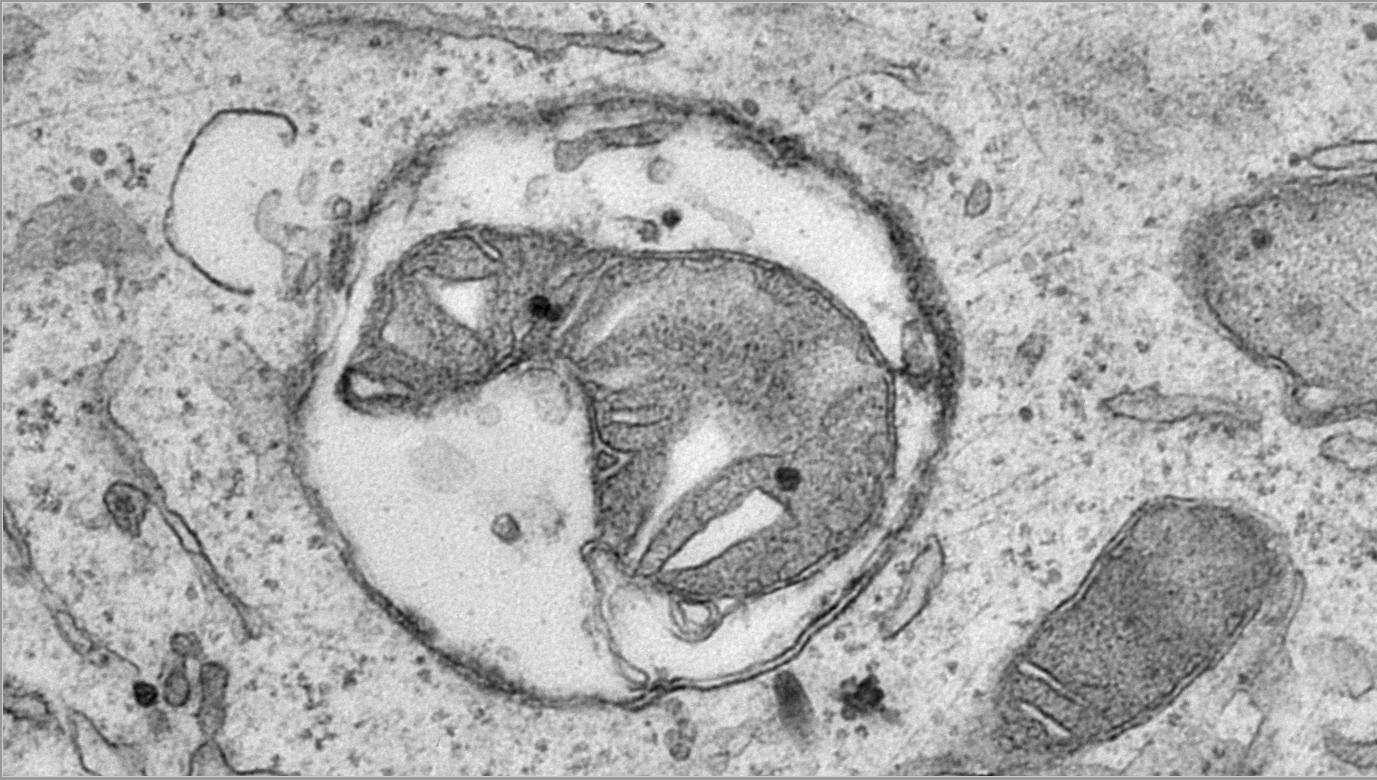
Zoë Van Acker, eerste auteur van de studie: “Het is spannend om nu antwoorden te hebben op deze vragen, te beginnen met de ontdekking dat het grootste deel van het DNA afkomstig is van mitochondriën, de energiecentrales van hersencellen. Normaal gesproken worden oude en beschadigde mitochondriën afgebroken en vervangen door nieuwe, maar als PLD3 niet goed werkt, kan het DNA zich ophopen en verstoppingen veroorzaken in het lysosomale systeem.”
De wetenschappers ontdekten dat het overtollige mitochondriale DNA lekt uit lysosomen, vergelijkbaar met een olielek. Dit lek zorgt ervoor dat bepaalde signaalroutes geactiveerd worden, die dit probleem echter nog verder versterken. Meer afval en celcomponenten worden toegevoegd aan de al overbelaste lysosomen. Als gevolg daarvan kunnen de lysosomen hun gebruikelijke afval, inclusief de schadelijke fragmenten die worden gevormd bij de ziekte van Alzheimer, onvoldoende snel afbreken. Deze verstoppingen zorgen ervoor dat deze schadelijke fragmenten zich versneld ophopen, wat leidt tot verdere schade aan de hersencellen en het risico om Alzheimer te ontwikkelen verhoogd.
Deze nieuwe bevindingen werpen meer licht op de complexe processen die betrokken zijn bij de ziekte van Alzheimer. Door beter te begrijpen hoe verstoppingen in het afvalophaal – en verwerkingssysteem van hersencellen tot Alzheimer kunnen leiden, kunnen wetenschappers mogelijk nieuwe behandelingen ontwikkelen om de ziekte te vertragen of zelfs te voorkomen.

Publicatie
Phospholipase D3 degrades mitochondrial DNA to regulate nucleotide signaling and APP metabolism. Van Acker, et al. Nature Communications, 2023. https://doi.org/10.1038/s41467-023-38501-w
India Jane Wise
Joran Lauwers
Over het VIB-KU Leuven Centrum voor Hersenonderzoek
Het VIB-KU Leuven Centrum voor Hersenonderzoek onderzoekt hoe hersencellen georganiseerd zijn en hoe ze met elkaar communiceren. Deze mechanismen blootleggen, geeft inzichten in wat er mis gaat bij hersenaandoeningen, zoals alzheimer, parkinson, ALS, en dystonie. Dit basiswerk moet uiteindelijk leiden tot nieuwe geneesmiddelen tegen deze ongeneeslijke aandoeningen.